Alcoolate
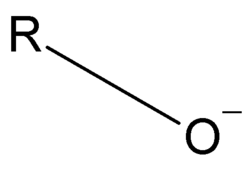
Un alcoolate (ou alkoxyde), de formule R-OModèle:Exp, est la base conjuguée d'un alcool. Son contre-ion peut être un atome métallique ou un radical organique.
Synthèse
Les alcoolates peuvent être synthétisés par oxydation de métaux alcalins, tel le sodium (Na) :
Ils peuvent également être synthétisés par réaction acido-basique avec une base très forte, comme l'hydrure de sodium.
Réactivité
Les alcoolates possèdent trois types de réactivité.
Comme base
Bases conjuguées des alcools, les alcoolates peuvent réaliser des réactions acido-basiques. Leur pKa est compris de manière générale entre 16 et 18, à l'exception des phénolates dont le pKa est plus proche de 10.
Comme nucléophile
L'atome d'oxygène est un site nucléophile, considéré comme « dur » dans la théorie HSAB.
Les alcoolates peuvent réagir avec des composés halogénés pour former des éthers, par la synthèse de Williamson :
Il est également possible d'obtenir des esters ou des tosylates.
Vis-à-vis de l'oxydation
Les ions alcoolates sont susceptibles d'être oxydés en radicaux alkoxyles par le dioxygène de l'air[1].
Nomenclature
Les alcoolates sont désignés par le suffixe -olate.
Notes et références
Articles connexes
- ↑ Erreur de référence : Balise
<ref>incorrecte : aucun texte n’a été fourni pour les références nomméesICO393